Hợp chất A có công thức MXx trong đó M chiếm 46,67% khối lượng (M là kim loại, X là phi kim ở chu kì 3). Trong hạt nhân M có số nơtron nhiều hơn số proton 4 hạt, còn X có số proton bằng số nơtron. Tổng số hạt proton của A là 58. Xác định M,X,A.

Những câu hỏi liên quan
Hợp chất H có công thức MX2 trong đó M chiếm 140/3% về khối lượng, X là phi kim ở chu kỳ 3, trong hạt nhân của M có số proton ít hơn số nơtron là 4; trong hạt nhân của X có số proton bằng số nơtron. Tổng số proton trong 1 phân tử A là 58. Cấu hình electron ngoài cùng của M là. A. 3d104s1. B. 3s23p4. C. 3d64s2. D. 2s22p4.
Đọc tiếp
Hợp chất H có công thức MX2 trong đó M chiếm 140/3% về khối lượng, X là phi kim ở chu kỳ 3, trong hạt nhân của M có số proton ít hơn số nơtron là 4; trong hạt nhân của X có số proton bằng số nơtron. Tổng số proton trong 1 phân tử A là 58.
Cấu hình electron ngoài cùng của M là.
A. 3d104s1.
B. 3s23p4.
C. 3d64s2.
D. 2s22p4.
Đáp án C
Tổng số proton trong MX2 là 58 hạt
→ ZM + 2.ZX = 58
Trong hạt nhân M có số notron nhiều hơn số hạt proton là 4 hạt
→ -ZM + NM = 4
Trong hạt nhân X, số notron bằng số proton → ZX = NX
MA =ZM + NM + 2.ZX + 2.NX
= (ZM + 2.ZX ) + NM + 2NX
= 58 + NM + 58 - ZM = 116 + NM- ZM
M chiếm 46,67% về khối lượng
![]()
![]()
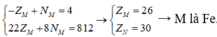
![]()
Cấu hình electron của M là [Ar]3d64s2.
Đúng 0
Bình luận (0)
Hợp chất H có công thức
M
X
2
trong đó M chiếm
140
3
%
về khối lượng, X là phi kim ở chu kỳ 3, trong hạt nhân của M có số proton ít hơn số nơtron là 4; trong hạt nhân của X có số proton bằng số nơtron. Tổng số proton trong 1 phân tử H là 58. Cấu hình electron ngoài cùng của M là A.
3
d
10
4
s
1
B. ...
Đọc tiếp
Hợp chất H có công thức M X 2 trong đó M chiếm 140 3 % về khối lượng, X là phi kim ở chu kỳ 3, trong hạt nhân của M có số proton ít hơn số nơtron là 4; trong hạt nhân của X có số proton bằng số nơtron. Tổng số proton trong 1 phân tử H là 58. Cấu hình electron ngoài cùng của M là
A. 3 d 10 4 s 1
B. 3 s 2 3 p 4
C. 3 d 6 4 s 2
D. 2 s 2 2 p 4
Chọn C
Tổng số proton trong MX2 là 58 hạt → ZM + 2.ZX = 58
Trong hạt nhân M có số nơtron nhiều hơn số hạt proton là 4 hạt → -ZM + NM = 4
Trong hạt nhân X, số nơtron bằng số proton → ZX = NX
MH =ZM + NM + 2.ZX + 2.NX = (ZM + 2.ZX ) + NM + 2NX = 58 + NM + 58 - ZM = 116 + NM - ZM

Đúng 0
Bình luận (0)
Hợp chất H có công thức MX2 trong đó M chiếm
140
3
% về khối lượng, X là phi kim ở chu kỳ 3, trong hạt nhân của M có số proton ít hơn số nơtron là 4; trong hạt nhân của X có số proton bằng số nơtron. Tổng số proton trong 1 phân tử H là 58. Cấu hình electron ngoài cùng của M là. A.
3
d
10
4
s
1
B.
3
s
2
3...
Đọc tiếp
Hợp chất H có công thức MX2 trong đó M chiếm 140 3 % về khối lượng, X là phi kim ở chu kỳ 3, trong hạt nhân của M có số proton ít hơn số nơtron là 4; trong hạt nhân của X có số proton bằng số nơtron. Tổng số proton trong 1 phân tử H là 58. Cấu hình electron ngoài cùng của M là.
A. 3 d 10 4 s 1
B. 3 s 2 3 p 4
C. 3 d 6 4 s 2
D. 2 s 2 2 p 4
Hợp chất A có công thức dạng \(MX_y\) trong đó M chiếm 46,67% về khối lượng. M là kim loại, X là phi kim có 3 lớp e trong nguyên tử. Hạt nhân M có n-p=4. Hạt nhân x có n'=p' (n,p,n',p' là số nơtron và proton của nguyên tử M và X). Tổng số proton trong \(MX_y\) là 58. Xác định các nguyên tử M và X
Hợp chất A có công thức dạng \(MX_y\) trong đó M chiếm 46,67% về khối lượng. M là kim loại, X là phi kim có 3 lớp e trong nguyên tử. Hạt nhân M có n-p=4. Hạt nhân x có n'=p' (n,p,n',p' là số nơtron và proton của nguyên tử M và X). Tổng số proton trong \(MX_y\) là 58. Xác định các nguyên tử M và X
$\dfrac{M}{Xy} = \dfrac{46,67}{53,33} \Rightarrow \dfrac{n + p}{y(n' + p')} = \dfrac{46,67}{53,33} = \dfrac{7}{8}$
Thay $n - p = 4$ và $n' = p'$ vào, ta có :
$\dfrac{2p+ 4}{2xp'} = \dfrac{7}{8} \Rightarrow 4(2p + 4) = 7xp'$
Tổng số proton trong MAx là 58 nên: p + xp’ = 58. Từ đây tìm được: p = 26 và xp’ = 32.
Do A là phi kim ở chu kì 3 nên 15 ≤ p’ ≤ 17. Vậy x = 2 và p’ = 16 thỏa mãn.
Vậy M là Fe và A là S; công thức của MAx là FeS2.
Đúng 3
Bình luận (1)
Hợp chất H có công thức là MAx, trong đó M chiếm 46,67% về khối lượng. M là kim loại, A là phi kim thuộc chu kì 3. Trong hạt nhân M có số hạt notron hơn số hạt proton là 4, trong hạt nhân của A có số proton và số notron bằng nhau. Tổng số proton trong là 58. Hai nguyên tố M và A là: A. Fe và S. B. Cr và Si C. Cr và S D. Fe và Si
Đọc tiếp
Hợp chất H có công thức là MAx, trong đó M chiếm 46,67% về khối lượng. M là kim loại, A là phi kim thuộc chu kì 3. Trong hạt nhân M có số hạt notron hơn số hạt proton là 4, trong hạt nhân của A có số proton và số notron bằng nhau. Tổng số proton trong là 58. Hai nguyên tố M và A là:
A. Fe và S.
B. Cr và Si
C. Cr và S
D. Fe và Si
M chiếm 46,67% về khối lượng:

Quan sát – phân tích: Hệ 5 ẩn gồm 4 phương trình không thể giải thông thường để tìm nghiện vì ta cần phải rút gọn nghiệm: Phương trình (2) chứa ẩn ZM và x. ZA từ phương trình (1); (3); (4) ta có thể đưa về 1 phương trình chứa 2 ẩn ZM và x
Z A → Đưa về hệ phương trình 2 ẩn.
Ta đưa được về hệ sau
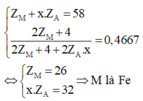
M là Fe nên x sẽ nhận giá trị từ 1 đến 3.
Từ x.ZA = 32 ta có các giá trị của ZA

Vậy H là FeS2
Đáp án A.
Đúng 0
Bình luận (0)
Hợp chất Y có công thức MX2 trong đó M chiếm 46,67% về khối lượng. Trong hạt nhân M có số nơtron nhiều hơn số proton là 4 hạt . Trong hạt nhân X, số nơtron bằng số proton. Tổng số proton trong MX2 là 58 hạt. Tìm AM và AX .
A. 26 và 16 B. 65 và 16 C. 56 và 32 D. 39 và 32
Một hợp chất có công thức MAx (trong đó M chiếm 46,667% veef khối lượng). A là phi kim, M là kim loại ở chu kì 3 (13 số proton nguyên tử A 18). Trong hạt nhân của M có số notron nhiều hơn số proton là 4, trong hạt nhân của A có số notron bằng số proton. Tổng số proton trong MAx là 58. Xác định số proton, số notron, tên nguyên tố hóa học của M, A và công thức hóa học của MAx mình đang cần chiều nay, nhờ mọi người nhé
Đọc tiếp
Một hợp chất có công thức MAx (trong đó M chiếm 46,667% veef khối lượng). A là phi kim, M là kim loại ở chu kì 3 (13 < số proton nguyên tử A < 18). Trong hạt nhân của M có số notron nhiều hơn số proton là 4, trong hạt nhân của A có số notron bằng số proton. Tổng số proton trong MAx là 58. Xác định số proton, số notron, tên nguyên tố hóa học của M, A và công thức hóa học của MAx
mình đang cần chiều nay, nhờ mọi người nhé
Trong hợp chất MAx thì M chiếm 46,67% về khối lượng nên ta có:
\(\dfrac{M_X}{A}=\dfrac{46,67}{53,33}\)→\(\dfrac{n+p}{x\left(n'+p\right)}=\dfrac{7}{8}\)(1)
Thay n – p = 4 và n’ = p’ vào (1) ta có: \(\dfrac{2p+4}{2xp'}=\dfrac{7}{8}\)
Tổng số proton trong MAx là 58 nên p +xp’= 58 (2)
Giải (1) và (2) ta có p= 26 và xp’ = 32
Do A là phi kim ở chu kì 3 nên 15 ≤ p’≤17.
Vậy x =2 và p’=16 thỏa mãn
Vậy M là Fe và A là S. Công thức phân tử FeS2.
Đúng 1
Bình luận (0)
Câu 1.1:Một hợp chất hữu cơ có công thức MAx,trong đó M chiếm 46,667% về khối lượng.M là kim loại,A là phi kim ở chu kỳ 3.Trong hạt nhân của M có số nơtron bằng số proton.Tổng số proton trong MAx là 58.xác định số proton,số nơtron,tên nguyên tố M,A và công thức MAxCâu 1.2:Một loại muối ăn(NaCl)có lẫn tạp chấtCaCl2,MgCl2,Na2SO4,MgSO4,CaSO4.Hãy trình bày cách loại các tạp chất để thu muối ăn tinh khiết
Đọc tiếp
Câu 1.1:Một hợp chất hữu cơ có công thức MAx,trong đó M chiếm 46,667% về khối lượng.M là kim loại,A là phi kim ở chu kỳ 3.Trong hạt nhân của M có số nơtron bằng số proton.Tổng số proton trong MAx là 58.xác định số proton,số nơtron,tên nguyên tố M,A và công thức MAx
Câu 1.2:Một loại muối ăn(NaCl)có lẫn tạp chấtCaCl2,MgCl2,Na2SO4,MgSO4,CaSO4.Hãy trình bày cách loại các tạp chất để thu muối ăn tinh khiết
Câu 1,2
Cho nước vào hỗn hợp, lọc bỏ phần không tan
Cho thêm dung dịch CaCl2 tới dư vào, lọc bỏ phần không tan
$CaCl_2 + Na_2SO_4 \to CaSO_4 + 2NaCl$
$CaCl_2 + MgSO_4 \to CaSO_4 + MgCl_2$
Dung dịch gồm : NaCl,MgCl2,Na2SO4,CaCl2
Cho dung dịch NaOH dư vào, lọc bỏ phần không tan
$MgCl_2 + 2NaOH \to Mg(OH)_2 + 2NaCl$
Dung dịch gồm : NaCl,Na2SO4,NaOH,CaCl2
Cho thêm dung dịch H2SO4 tới dư vào, lọc bỏ phần không tan, cho bay hơi dung dịch
$2NaOH + H_2SO_4 \to Na_2SO_4 + 2H_2O$
$CaCl_2 + H_2SO_4 \to CaSO_4 + 2HCl$
Chất rắn khan gồm : Na2SO4,NaCl
Cho dung dịch BaCl2 tới dư vào, lọc dung dịch
$BaCl_2 + Na_2SO_4 \to BaSO_4 + 2NaCl$
Dung dịch gồm : BaCl2,NaCl
Cho dung dịch H2SO4 tới dư vào, cô cạn dung dịch . Ta được naCl tinh khiết
$BaCl_2 + H_2SO_4 \to BaSO_4 + 2HCl$
Đúng 2
Bình luận (0)
TK: nếu là 67 thì
1.1
M là Fe (26); A là S (16) công thức là FeS2
Giải thích các bước giải:
Ta có %M=46,67% -> %A=53,33%
Ta có : M=n+p; A=n'+p'
-> (n+p)/(x(n'+p'))=46,67/53,33=7:8
Vì n-p=4 -> n=4+p
-> (2p+4)/2xp'=7/8 -> 7xp'-8p=16
Tổng số proton =p+xp'=58 -> p=26; xp'=32
Vì A là phi kim thuộc chu kì 3 nên 15 <= p' <=17 (P; S; Cl)
Với x=2 -> p'=16
Vậy M là Fe; A là S công thức là FeS2
1.2
cho vào lượng dư dung dịch BaCl2
MgSO4+BaCl2=>BaSO4+MgCl2
lọc bỏ kết tủa tiếp tục cho vào lượng dư Na2CO3
MgCl2+Na2CO3=>MgCO3+2NaCl
BaCl2+Na2CO3=>BaCO3+2NaCl
CaCl2+Na2CO3=>CaCO3+2NaCl
lọc bỏ kết tủa, dung dịch gồm NaCl Na2CO3 dư
cho HCl dư vào
2HCl+Na2CO3=>2NaCl+H2O+CO2
đun nhẹ dung dịch cho HCl dư bay hơi cô cạn dung dịch thu được NaCl tinh khiết
Đúng 0
Bình luận (0)















